Che cosa è la mielofibrosi
 La mielofibrosi è una rara malattia cronica del midollo osseo che appartiene al gruppo delle malattie mieloproliferative croniche (che comprendono anche la policitemia vera e la trombocitemia essenziale).
La mielofibrosi è una rara malattia cronica del midollo osseo che appartiene al gruppo delle malattie mieloproliferative croniche (che comprendono anche la policitemia vera e la trombocitemia essenziale).
Il termine “mieloproliferative” indica che si tratta di un’alterazione che si verifica nelle cellule del midollo osso (“mielo”) e che induce una proliferazione eccessiva di altre cellule.
 Il midollo osseo contiene le cellule staminali, ossia le cellule non mature, che possono trasformarsi in vari tipi di altre cellule attraverso un processo di maturazione detto anche differenziazione. Si definiscono emopoietiche (dal greco “che creano il sangue”), quelle cellule staminali che danno origine alle cellule mature del sangue: globuli bianchi (o leucociti), globuli rossi (o eritrociti) e piastrine (o trombociti).
Il midollo osseo contiene le cellule staminali, ossia le cellule non mature, che possono trasformarsi in vari tipi di altre cellule attraverso un processo di maturazione detto anche differenziazione. Si definiscono emopoietiche (dal greco “che creano il sangue”), quelle cellule staminali che danno origine alle cellule mature del sangue: globuli bianchi (o leucociti), globuli rossi (o eritrociti) e piastrine (o trombociti).
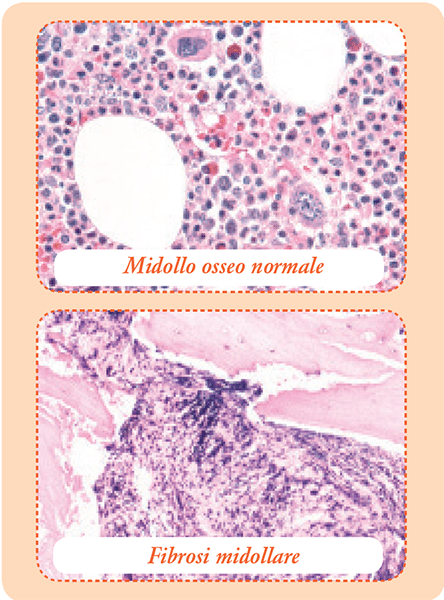
La mielofibrosi è un’alterazione di queste cellule staminali, così chiamata perché, se si osserva al microscopio il midollo osseo, si nota la graduale comparsa di un tessuto fibroso (un insieme di fibre isolate o intrecciate tra di loro) che modifica definitivamente la struttura del midollo osseo stesso non consentendogli più di funzionare correttamente.
Esistono due forme di mielofibrosi:
Primaria (o idiopatica, dal greco “malattia che origina da se stessa”).
Così chiamata perché non è dovuta ad altre malattie o cause esterne.
Secondaria, evoluzione di un’altra malattia mieloproliferativa cronica, come la policitemia vera o la trombocitemia essenziale.
Le caratteristiche con cui si manifesta la mielofibrosi sono diverse da persona a persona e possono dar luogo negli anni a situazioni cliniche molto variabili e complesse
Le cause della mielofibrosi non sono state ancora del tutto chiarite ma la malattia si associa ad alterazioni specifiche del DNA che colpiscono la cellula staminale e ne alterano il comportamento.
Le principali mutazioni sinora identificate sono tre: in circa il 50-60% dei casi è presente una mutazione del gene JAK2 (Janus Activated Kinase 2), nel 30% dei casi sono presenti mutazioni del gene CALR (calreticulina), quasi esclusivamente in pazienti che non hanno mutazioni JAK2 o MPL, nel 5% dei casi sono presenti alterazioni del gene MPL che possono essere presenti anche in un’altra malattia mieloproliferativa cronica, la trombocitemia essenziale. Inoltre, indipendentemente dalle mutazioni coinvolte, in tutti i pazienti si nota una iperattivazione dei meccanismi dipendenti da JAK2 che controllano la proliferazione delle cellule del sangue.
Contenuto
EPIDEMIOLOGIA (DIFFUSIONE)
La mielofibrosi è una malattia rara, in Italia si calcola che ci siano da 5 a 15 nuovi casi ogni milione di abitanti, che si traducono in circa 350 nuovi casi all’anno.
La malattia può colpire allo stesso modo sia i maschi che le femmine. Nella maggior parte dei casi colpisce pazienti tra i 60 e i 70 anni di età.
Nel 15% dei casi può interessare persone con meno di 55 anni, mentre i casi pediatrici sono rarissimi. La mielofibrosi è una malattia che si acquisisce nel corso della vita quindi non è ereditaria per cui non c’è il rischio di trasmetterla ai propri figli. Come per altre malattie, ad esempio il diabete e l’ipertensione, si può ereditare dai genitori e trasmettere ai figli solo una generica predisposizione verso la malattia. In questi casi si parla di “familiarità”.
In termini pratici, le persone che hanno un parente stretto malato hanno un modesto aumento del rischio di sviluppare la stessa o un’altra delle malattie mieloproliferative, ma non sono ancora note indagini cliniche o di laboratorio di natura preventiva.
Principali alterazioni nella mielofibrosi
- Aumento del numero e modifica della forma dei megacariociti, che sono le cellule che producono le piastrine (così chiamate perché sono le più grandi tra le cellule del midollo osseo) e che derivano dalle cellule staminali emopoietiche.
- Fibrosi del midollo osseo.
- Aumento delle dimensioni della milza (splenomegalia) e talora del fegato (epatomegalia).
- Presenza nel sangue di globuli rossi e di globuli bianchi non maturi.
- Alterazioni del numero dei globuli bianchi, delle piastrine e dei globuli rossi.
ANDAMENTO NEL TEMPO
La mielofibrosi è una malattia cronica che può peggiorare più o meno lentamente nell’arco di diversi anni, con modalità variabili a seconda del paziente. In genere la fase iniziale della malattia consiste in un danno alla struttura del midollo osseo: in particolare i megacariociti aumentano di numero e cambiano forma.
Questa fase si definisce fase precoce, o pre-fibrotica, perché non è presente ancora la fibrosi del midollo osseo.
In una seconda fase (fase avanzata), compare la fibrosi midollare e si può avere una fuoriuscita di cellule staminali immature dal midollo osseo. Queste, attraverso il sangue, raggiungono la milza e il fegato, dove si accumulano.
Talvolta può accadere che per anni il paziente rimanga stabile presentando solamente lievi alterazioni del midollo osseo e un aumento delle piastrine.
Nella maggioranza dei casi, quando la malattia si manifesta sono già presenti le alterazioni tipiche:
- fibrosi del midollo osseo
- anemia (diminuzione dei globuli rossi nel sangue)
- numero troppo alto o troppo basso di globuli bianchi e di piastrine
- ingrossamento della milza.
In alcuni casi (10-15 su 100) la mielofibrosi può evolvere in una patologia più severa come la leucemia acuta.
Il passaggio da mielofibrosi a leucemia acuta è generalmente accompagnato da un aumento rapido e notevole nel sangue di globuli bianchi immaturi (chiamati blasti), i quali non riuscendo più a maturare e a diventare cellule funzionanti in modo corretto, impediscono la produzione di tutte le cellule del sangue.
La leucemia acuta ha pesanti conseguenze per il paziente: oltre a un aggravamento delle sue condizioni generali di salute, aumenta sensibilmente il pericolo di infezioni gravi e di emorragie.
Il criterio generale per sospettare la diagnosi di una leucemia acuta è che il numero dei blasti sia maggiore del 20% del totale delle cellule presenti nel sangue e nel midollo osseo.
PROGNOSI
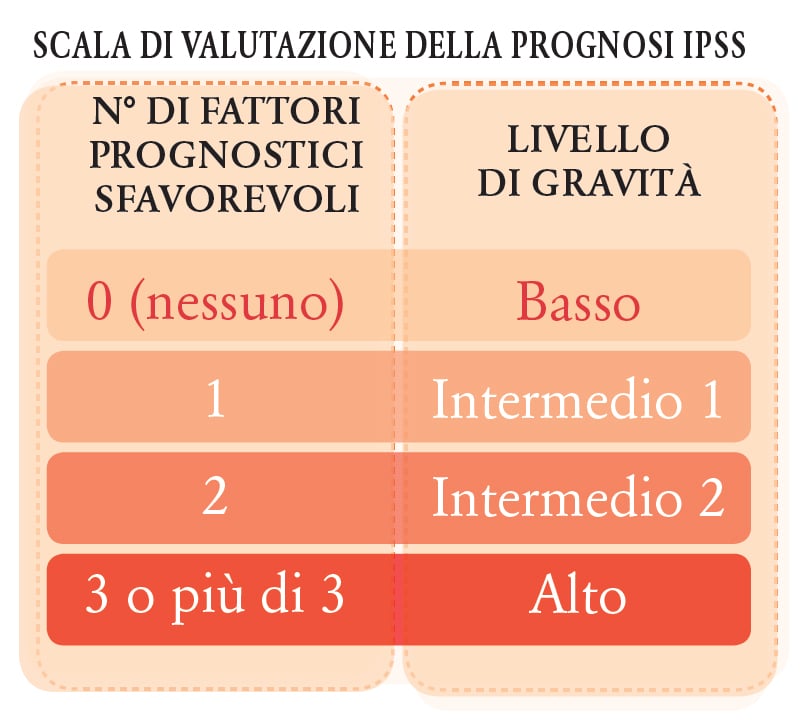
Attualmente la prognosi di un paziente con mielofibrosi primaria, ossia la previsione di come la malattia evolverà nel tempo, viene definita in base alla scala di valutazione della prognosi IPSS (International Prognostic Scoring System), in cui si deve valutare la presenza o meno di ciascuno dei seguenti fattori:
- Anemia (valore di emoglobina nel sangue inferiore a 10 grammi per decilitro)
- Leucocitosi (n. di globuli bianchi superiore a 25.000 per millimetro cubo di sangue)
- Età avanzata (età superiore a 60 anni)
- Presenza di blasti in percentuale uguale o superiore all’1% nelle cellule del sangue
- Presenza di sintomi generali (per esempio febbre non dovuta a infezioni, sudorazioni notturne abbondanti, dimagrimento negli ultimi 6 mesi pari o superiore al 10% del peso corporeo).
A seconda del numero di fattori presenti, viene definito il livello di gravità della malattia
Quali sono i sintomi?
QUADRO COMPLESSIVO
Un quarto dei malati con mielofibrosi non accusa alcun particolare sintomo al momento della visita, cioè è asintomatico.
Generalmente il primo segnale viene da un normale esame del sangue in cui si esegue il conteggio delle cellule (chiamato emocromo), che indica la presenza di valori alterati.
In altre situazioni invece sono presenti dei sintomi generici, quali stanchezza inusuale, o altri più tipici della mielofibrosi, quali disturbi addominali come un fastidio causato da un ventre gonfio e/o una sensazione di stomaco eccessivamente pieno soprattutto dopo i pasti, che sono dovuti al coinvolgimento di alcuni organi, soprattutto all’ingrossamento della milza.
DISTURBI GENERALI
Si tratta di sintomi che si possono manifestare anche in molte altre malattie, ma che nella mielofibrosi, possono diventare debilitanti e influire sulla qualità di vita del paziente impedendogli talvolta di svolgere le abituali attività lavorative e quotidiane e influenzando negativamente la normale vita di relazione.
Il sintomo principale è la sensazione di profonda stanchezza e debolezza (in inglese, “fatigue” che in italiano si può tradurre con “astenia”) che si manifesta anche senza aver fatto particolari sforzi; si possono anche avere mancanza di appetito, dolori muscolari alle gambe, difficoltà di concentrazione, alterazioni del sonno, ansia e depressione.
Sintomi generali più comuni
- Sensazione di debolezza, anche senza sforzi eccessivi (fatigue/astenia)
- Profonda stanchezza, difficoltà talora a respirare, alterazioni della funzione cardiaca dovute a anemia (valori bassi di emoglobina, con riduzione del numero di globuli rossi)
- Febbre o febbricola (non causata da un’infezione)
- Dimagrimento (perdita di almeno il 10% del proprio peso negli ultimi 6 mesi)
- Sudorazione notturna molto abbondante
- Prurito (diffuso in tutto il corpo, e che peggiora con il contatto con l’acqua)
- Dolori alle ossa e/o alle articolazioni
In taluni casi le manifestazioni possono essere più complesse e difficili da interpretare anche da parte del medico.
DISTURBI DOVUTI A DANNI AGLI ORGANI
L’ingrossamento della milza (detto splenomegalia) è la manifestazione più caratteristica della mielofibrosi, si verifica in quasi tutti i malati ed è responsabile di una serie di disturbi, prevalentamente gastrointestinali, elencati di seguito.
- Pesantezza addominale
- Difficoltà digestive
- Sazietà precoce
- Dolori addominali
- Diarrea o stitichezza
- Tosse secca (senza catarro) spesso accompagnata da senso di fastido alla spalla sinistra
- Disturbi urinari
- Difficoltà a trovare una posizione durante il sonno o in poltrona
- Difficoltà a piegarsi e/o ad effettuare un certo tipo di attività
- Ingrossamento delle gambe per edema (accumulo di liquido nei tessuti)
 La milza si ingrossa a causa dell’accumulo in questo organo di cellule fuoriuscite dal midollo osseo (emopoiesi extramidollare).
La milza si ingrossa a causa dell’accumulo in questo organo di cellule fuoriuscite dal midollo osseo (emopoiesi extramidollare).
La milza ingrossata preme sullo stomaco e sull’intestino, impedendo loro di funzionare regolarmente.
Il paziente avverte difficoltà nella digestione, sensazioni di pesantezza di stomaco, fastidio a livello dell’addome e sazietà anche dopo aver mangiato poco (questo è uno dei motivi per cui il paziente dimagrisce molto), dolori addominali, nonché funzioni intestinali irregolari (con episodi sia di diarrea che di stitichezza).
In alcuni casi la milza è così ingrandita che occupa gran parte dell’addome fino ad arrivare a comprimere i polmoni (provocando tosse secca e dolore alla spalla sinistra) e il rene (determinando difficoltà a urinare).
DISTURBI DA ALTERAZIONI DEL MIDOLLO OSSEO
Si tratta di sintomi, descritti nella tabella sottostante, che sono conseguenti ad una incapacità del midollo osseo di produrre quantità normali di globuli rossi, globuli bianchi e piastrine.
A causa di una diminuzione dei globuli rossi nel sangue e dell’emoglobina in essi contenuta, oltre la metà dei malati è anche anemica: ciò provoca stanchezza, debolezza, colorito pallido, inappetenza, difficoltà di respirazione e battito del cuore accelerato.
In alcuni pazienti affetti da mielofibrosi i globuli bianchi possono aumentare enormemente (leucocitosi); altre volte invece si verifica il processo inverso e il numero di globuli bianchi nel sangue può ridursi anche notevolmente (leucopenia), rendendo il paziente più sensibile alle infezioni. Questo accade perché i globuli bianchi sono componenti del sistema immunitario che difende il nostro organismo dall’attacco delle sostanze estranee e che nella mielofibrosi non funziona in modo ottimale.
Anche la quantità di piastrine nel sangue può essere alterata, con valori sia troppo bassi sia troppo alti. In particolare un calo di piastrine è responsabile di emorragie a livello della pelle (con formazione di piccole chiazze rossastre) e della bocca, oppure di perdite di sangue dal naso.
COMPLICAZIONI PRINCIPALI
Tra le complicazioni più rischiose per i pazienti con mielofibrosi ci sono le trombosi, disturbi provocati da un coaugulo, detto trombo, che ostruisce un vaso sanguigno, impedendo al sangue di circolare regolarmente. Il trombo si forma nelle vene o nelle arterie a causa di una coagulazione del sangue che avviene in maniera scorretta per la presenza di piastrine alterate.
Nella mielofibrosi, gli episodi di trombosi si verificano in circa il 7% dei pazienti.
 I trombi possono essere arteriosi (cioè nei vasi che portano il sangue agli organi) oppure venosi (cioè nei vasi che riportano il sangue dagli organi verso il cuore). I primi sono generalmente più gravi dei secondi.
I trombi possono essere arteriosi (cioè nei vasi che portano il sangue agli organi) oppure venosi (cioè nei vasi che riportano il sangue dagli organi verso il cuore). I primi sono generalmente più gravi dei secondi.
A volte, sebbene raramente, le trombosi nei pazienti affetti da mielofibrosi si possono sviluppare in sedi anomale come i vasi sanguigni addominali che portano il sangue al fegato e alla milza. In questo caso si parla di trombosi splancnica.
Gli interventi chirurgici possono aumentare il rischio di sviluppare trombosi, quindi è importante preparare molto bene il paziente ad un intervento chirurgico, grazie a una stretta collaborazione tra chirurgo ed ematologo, per ridurre al minimo il rischio trombotico e quello emorragico legati all’intervento, a volte anche con l’assunzione di farmaci specifici.
Un’altra complicazione della mielofibrosi, più frequente se la milza è molto ingrossata, è l’infarto splenico (ossia un infarto a livello della milza), che viene provocato dall’ostruzione di un’arteria che porta sangue all’organo. Il malato lamenta un dolore improvviso e molto forte al fianco sinistro dove si trova la milza; talvolta le fitte dolorose sono accompagnate da febbre e nausea. In presenza di questi sintomi il medico curante potrà richiedere un’ecografia dell’addome, che potrà mettere in evidenza le tipiche alterazioni dell’organo associate con l’infarto. In genere questi sintomi passano in pochi giorni, ma nel caso in cui i farmaci antidolorifici non facciano effetto può essere necessario il ricovero in ospedale. Se la milza fosse troppo danneggiata è necessario asportarla con un intervento chirurgico.
Infine, un evento abbastanza frequente legato alla riduzione delle cellule ematiche e al loro elevato ricambio è la formazione di calcoli renali, che sono piccoli depositi di sali minerali che si formano nelle vie urinarie. Nel caso della mielofibrosi si sviluppano per un eccesso di acido urico nel sangue e possono dar luogo a episodi di dolore intenso (coliche) e talvolta impedire al rene di funzionare normalmente.
EFFETTI SULLA VITA QUOTIDIANA
La mielofibrosi, nei suoi stadi più avanzati, può avere un forte impatto sulla qualità di vita di chi ne è affetto.
La situazione complessiva può essere aggravata dal fatto che la mielofibrosi colpisce per lo più gli anziani, persone di solito più fragili, che spesso assumono farmaci per altri disturbi cronici e che, rispetto alla popolazione generale, hanno un rischio maggiore di sviluppare malattie a carico del cuore e dei vasi sanguigni (il cosiddetto rischio cardiovascolare).
 Nei casi in cui si sviluppi una profonda astenia (profusa stanchezza) e/o una splenomegalia massiva, la mielofibrosi può impedire di compiere una serie di attività quotidiane che di norma vengono svolte senza difficoltà, come camminare, salire le scale, rifare il letto, fare la doccia e cucinare. La malattia può anche influenzare negativamente sia la vita lavorativa che le relazioni sociali.
Nei casi in cui si sviluppi una profonda astenia (profusa stanchezza) e/o una splenomegalia massiva, la mielofibrosi può impedire di compiere una serie di attività quotidiane che di norma vengono svolte senza difficoltà, come camminare, salire le scale, rifare il letto, fare la doccia e cucinare. La malattia può anche influenzare negativamente sia la vita lavorativa che le relazioni sociali.
Nello specifico, anche se non ci sono particolari restrizioni lavorative, in caso di forte anemia (emoglobina inferiore a 10 grammi per decilitro) o di ingrossamento della milza molto marcato, alcune mansioni pesanti non sono praticabili, sia per la generale debolezza, sia per non sforzare troppo i muscoli addominali per il rischio di provocare lesioni alla milza ingrossata.
Inoltre, dato che il malato spesso ha poco appetito, problemi di sonno, difficoltà di concentrazione, stress, ansia e depressione, i rapporti con familiari, amici e colleghi possono diventare problematici e l’individuo tende a isolarsi perché condurre una vita sociale richiede troppa fatica.
In conclusione i disturbi della mielofibrosi possono essere molto debilitanti e condizionare notevolmente la vita quotidiana del malato, per cui non vanno mai sottovalutati, parlandone subito al proprio medico e facendosi consigliare i rimedi più opportuni.
Diagnosi
PRINCIPI GENERALI
 La diagnosi di mielofibrosi è piuttosto complessa e non esiste un unico esame che permette di confermarla, perché si tratta di un disturbo variabile da paziente a paziente che può essere spesso confuso con altre malattie croniche del midollo, come le altre malattie mieloproliferative, e con la leucemia mieloide cronica.
La diagnosi di mielofibrosi è piuttosto complessa e non esiste un unico esame che permette di confermarla, perché si tratta di un disturbo variabile da paziente a paziente che può essere spesso confuso con altre malattie croniche del midollo, come le altre malattie mieloproliferative, e con la leucemia mieloide cronica.
La diagnosi inizia con la raccolta di informazioni sulle condizioni di salute dell’individuo, appurando se ha avuto altre malattie croniche del sangue (policitemia vera o trombocitemia essenziale) o alterazioni nelle analisi del sangue, se è recentemente dimagrito, se soffre o ha mai sofferto di trombosi o di emorragie, se prova grave stanchezza e se suda abbondantemente durante il sonno.
In secondo luogo si passa alla visita vera e propria, che consente di rilevare l’eventuale ingrossamento della milza e il pallore della pelle. Anche se è spesso presente, l’ingrossamento della milza non significa per forza mielofibrosi, perché si può riscontrare anche in altre malattie del sangue o del fegato.
Per diagnosticare una mielofibrosi primaria è comunque necessario sottoporre il paziente a una serie di esami differenti, classificati come di seguito.
ANALISI DEL SANGUE
Anche se nella mielofibrosi in fase iniziale l’esame che conta le cellule ematiche (chiamato comunemente emocromo) può risultare normale, spesso si evidenzia un aumento delle piastrine. Con il progredire della malattia si può osservare un considerevole calo, o al contrario, un aumento di globuli bianchi e di piastrine, e anche una riduzione di emoglobina (anemia). È inoltre molto importante analizzare il sangue al microscopio in maniera da osservare la forma delle cellule: infatti in caso di mielofibrosi si notano globuli rossi tipicamente deformati “a lacrima” (dacriociti), che indicano la presenza di fibrosi midollare. L’esame al microscopio evidenzia nel sangue anche molte cellule immature: globuli bianchi che di solito si trovano esclusivamente nel midollo osseo, piastrine di dimensioni giganti e globuli rossi non maturi.
Nel sangue si può misurare anche la lattato deidrogenasi (LDH), una sostanza normalmente presente in quantità estremamente piccole che aumenta molto nelle malattie del sangue, in particolare nella mielofibrosi. L’LDH viene prodotta in seguito alla distruzione delle cellule ematiche.
BIOPSIA OSSEA
 È l’esame principale per diagnosticare la mielofibrosi perché permette di controllare direttamente le condizioni del midollo osseo.
È l’esame principale per diagnosticare la mielofibrosi perché permette di controllare direttamente le condizioni del midollo osseo.
Si preleva un campione di tessuto del midollo osseo e lo si analizza al microscopio. In tal modo è possibile vedere se ci sono alterazioni nel numero e nelle forma delle cellule del midollo, e verificare la presenza di fibrosi
Si possono fare due tipi di prelievi: biopsia osteomidollare e aspirato midollare.
- Biopsia osteomidollare. È un esame che non richiede il ricovero, ma si esegue in anestesia locale, e può essere leggermente fastidioso. Consiste nel prelevare un piccolo campione di tessuto di midollo osseo (2-3 cm di lunghezza e 3 mm di diametro) dalla parte superiore e posteriore dell’osso dell’anca (cresta iliaca posteriore). Si inserisce un ago particolare direttamente nell’osso per un paio di centimetri, e si preleva così un piccolo frammento di tessuto da analizzare.
- Aspirato midollare. Consiste nel prelievo di una piccola quantità di sangue dal midollo. In genere si effettua in anestesia locale, utilizzando un ago corto e robusto. Il prelievo viene quasi sempre effettuato nella stessa zona della biopsia, solo molto raramente a livello dell’osso dello sterno (parte anteriore del torace). L’aspirazione è breve e può dare dolore.
ANALISI GENETICHE
Negli ultimi anni, i risultati di queste analisi hanno consentito di approfondire le conoscenze riguardo alla malattia, aiutando a definirla con sempre maggiore precisione.
L’analisi citogenetica valuta il cosiddetto cariotipo della cellula, ossia il numero e la forma dei suoi cromosomi. Questo esame evidenzia che in circa il 40% dei pazienti con mielofibrosi le cellule del sangue danneggiate possiedono cromosomi con una struttura difettosa.
Non si tratta però di anomalie congenite, ossia non sono presenti già alla nascita, ma si sviluppano successivamente, probabilmente nel momento in cui compare la mielofibrosi.
Tra le alterazioni più comuni c’è la mancanza di una porzione del cromosoma 13 o 20. Inoltre forme di malattia più gravi e con un decorso più rapido del solito sembrano dovute all’esistenza di specifici danni cromosomici.
Le analisi molecolari ricercano invece la presenza di mutazioni geniche, ossia di variazioni dei geni, che sono le unità contenenti le informazioni genetiche all’interno dei cromosomi. Anche le mutazioni non sono congenite nella mielofibrosi e si verificano esclusivamente nelle cellule del sangue danneggiate.
La mutazione del gene JAK2 è quella più diffusa nei malati di mielofibrosi, anche se compare pure in quasi tutti i pazienti con policitemia vera e nella metà circa di quelli con trombocitemia essenziale. Questa mutazione è responsabile della produzione di una proteina JAK2 difettosa che, non funzionando bene, stimola il midollo osseo a produrre in continuazione nuove cellule del sangue. La scoperta delle mutazioni geniche, e quella del gene JAK2 in particolare, e del loro ruolo nelle malattie mieloproliferative croniche come la mielofibrosi ha spinto a ricercare farmaci innovativi che siano in grado di bloccare selettivamente queste proteine malfunzionanti (vedi il capitolo sulla terapia).
CRITERI DIAGNOSTICI
Data la complessità nel diagnosticare la mielofibrosi primaria, per facilitare il compito dell’ematologo nel 2008 l’Organizzazione Mondiale della Sanità ha messo a punto una serie di criteri, che sono stati suddivisi in maggiori e minori.


La diagnosi di mielofibrosi primaria si basa sulla presenza di tutti i criteri maggiori e di almeno due tra i criteri minori.
Sono stati inoltre stabiliti una serie di criteri anche per diagnosticare la mielofibrosi post-trombocitemica e post-policitemica, che sono:
- Fibrosi del midollo osseo.
- Milza ingrossata
- Anemia
- Leucoeritroblastosi
- LDH aumentata
- Comparsa di sintomi costituzionali
Terapia
PERCORSO TERAPEUTICO
Data la variabilità con cui si manifesta la mielofibrosi, il percorso terapeutico non è uguale per tutti i pazienti.
Per esempio, quando i sintomi sono assenti oppure ci sono solo modeste alterazioni dell’emocromo non è sempre necessario assumere medicinali.
Quando invece la malattia è attiva esistono diverse possibilità che vanno scelte tenendo conto delle caratteristiche individuali del paziente e di quelle della malattia stessa.
L’unica terapia curativa è il trapianto di midollo osseo che però viene eseguito solo su un numero molto limitato di malati essendo una procedura complicata e gravata da notevoli rischi per la salute soprattutto nelle fasce di età più avanzate.
I medicinali tradizionali vengono impiegati essenzialmente per il trattamento dei disturbi provocati dall’anemia e dall’ingrossamento della milza, ma sono poco efficaci sui sintomi correlati alla mielofibrosi.
Accanto a essi esistono diversi farmaci innovativi, alcuni già disponibili, altri ancora in corso di sperimentazione. In ogni caso, che si assumano o meno medicinali, il paziente va sempre tenuto sotto controllo mediante visite e analisi del sangue periodiche (da una volta al mese a una ogni 3-4 mesi, in relazione al quadro clinico e al tipo di terapia), in maniera da rilevare tempestivamente non solo qualsiasi peggioramento del suo stato di salute ma anche la sua risposta alle terapie.
TRAPIANTO DI MIDOLLO OSSEO
Obiettivo del trapianto è di eliminare la malattia e ripristinare le normali funzioni del midollo osseo iniettando cellule staminali emopoietiche sane in grado di produrre tutte le cellule ematiche.
Si realizza con cellule staminali emopoietiche prelevate dal sangue o direttamente dal midollo di un donatore (trapianto allogenico) preferibilmente scelto in ambito familiare perché deve essere compatibile, cioè avere caratteristiche il più possibile simili al ricevente. Se in famiglia non è disponibile un donatore, si ricorre ai registri di donatori non familiari.
Prima di ricevere le cellule staminali, il paziente viene sottoposto a un trattamento con radiazioni e/o con farmaci per distruggere completamente le cellule del midollo malato e quindi per permettere che il suo organismo accetti le cellule staminali del donatore.
Tali terapie di preparazione, riducendo le difese immunitarie del ricevente, comportano un aumento delle infezioni e delle reazioni tossiche a livello dell’apparato gastrointestinale e del fegato, rappresentando così uno dei motivi per cui il trapianto è tuttora riservato a un numero limitato di pazienti. Il rischio di un insuccesso viene ulteriormente aggravato dalla complicazione più grave del trapianto allogenico, la malattia del trapianto contro l’ospite (GVHD, dall’inglese Graft Versus Host Disease).
La GVDH è provocata dal fatto che, insieme alle cellule staminali, vengono iniettate anche cellule del sistema immunitario del donatore che “aggrediscono” i tessuti del ricevente riconoscendoli come estranei.
Pertanto, anche se rappresenta l’unica opportunità per guarire la mielofibrosi, oggi il trapianto di cellule staminali emopoietiche viene consigliato solo ai pazienti più giovani (con meno di 60-65 anni) con malattia più grave (punteggio IPSS “Intermedio 2” oppure “Alto”).
TERAPIE TRADIZIONALI
La scelta di quale strategia adottare dipende essenzialmente dall’età dell’individuo, dalla prognosi della malattia e dalla presenza di altri disturbi, per esempio quelli cardiaci e renali.
Le terapie tradizionali sono rivolte principalmente al trattamento dell’anemia e dell’ingrossamento della milza, che spesso si manifestano insieme.
Tuttavia con questi farmaci il miglioramento dei sintomi generali correlati alla malattia è limitato.
TRATTAMENTO DELL’ANEMIA
 Il trattamento dell’anemia è necessario solamente nei pazienti che hanno un contenuto di emoglobina nel sangue estremamente basso (meno di 10 grammi per decilitro). In genere, dato che la terapia impiega diverso tempo per fare effetto, le analisi del sangue per controllare se l’anemia è migliorata si eseguono dopo alcuni mesi dall’inizio del trattamento.
Il trattamento dell’anemia è necessario solamente nei pazienti che hanno un contenuto di emoglobina nel sangue estremamente basso (meno di 10 grammi per decilitro). In genere, dato che la terapia impiega diverso tempo per fare effetto, le analisi del sangue per controllare se l’anemia è migliorata si eseguono dopo alcuni mesi dall’inizio del trattamento.
Nei casi più gravi può essere necessario ricorrere al trattamento trasfusionale.
La somministrazione di androgeni e di eritropoietina/darbopoietina provoca pochi effetti collaterali.
I farmaci immunomodulatori come talidomide/lenalidomide sono efficaci sull’anemia e in genere molto poco sull’ingrossamento della milza, ma il loro uso è gravato da molti effetti collaterali, per cui si usano raramente.
Il cortisone in alcuni casi può dare un miglioramento transitorio dell’anemia oltre che dei sintomi. Il suo uso a lungo termine può dare effetti collaterali (osteopenia, infezioni, ecc.).
TRATTAMENTO DELLA SPLENOMEGALIA
Una terapia per ridurre le dimensioni della milza va prevista quando si nota un costante aumento delle dimensioni della milza durante le visite di controllo, disturbi gastrointestinali, dolori addominali e in generale quando la milza supera le dimensioni di 5-10 cm dall’arcata costale.
Come prima scelta, nella pratica clinica, si usano i citostatici, farmaci che bloccano o rallentano la crescita delle cellule, di solito impiegati nella terapia dei tumori (chemioterapici). Tra questi il più diffuso è l’idrossiurea.
Nei pazienti in cui l’idrossiurea non funziona si possono scegliere altri farmaci, tra cui melfalan, busulfano, etoposide o interferone, anche se le probabilità di successo terapeutico sono piuttosto basse.
Nei casi in cui nessun farmaco riesca a normalizzare le dimensioni della milza e i sintomi sono così gravi da peggiorare la qualità di vita del paziente, si può optare per la rimozione chirurgica della milza o, in pochi casi selezionati, per una radioterapia specifica (irradiando l’area della milza per ridurre le sue dimensioni). Si tratta tuttavia di scelte da valutare attentamente per i numerosi rischi legati a queste procedure, che quindi si eseguono solo in casi molto selezionati anche perché non garantiscono la completa scomparsa dei disturbi.
TERAPIE INNOVATIVE – INIBITORI DI JAK
La scoperta, nel 2005, della mutazione del gene JAK2, è stata un grande stimolo per lo studio di nuovi farmaci in grado di trattare le neoplasie mieloproliferative che in molti casi presentano questa mutazione.
 Sono quindi stati sviluppati una serie di farmaci innovativi, chiamati inibitori di JAK, che hanno la capacità di inibire selettivamente le proteine della famiglia JAK che sono iperattivate in malattie come la mielofibrosi, ma anche nelle altre malattie croniche mieloproliferative (trombocitemia essenziale e policitemia vera).
Sono quindi stati sviluppati una serie di farmaci innovativi, chiamati inibitori di JAK, che hanno la capacità di inibire selettivamente le proteine della famiglia JAK che sono iperattivate in malattie come la mielofibrosi, ma anche nelle altre malattie croniche mieloproliferative (trombocitemia essenziale e policitemia vera).
In particolare, l’inibitore di JAK1 e di JAK2, ruxolitinib, capostipite della classe, dal 2014 è stato autorizzato in Italia con l’indicazione al trattamento della splenomegalia o dei sintomi correlati alla malattia in pazienti adulti con mielofibrosi primaria, mielofibrosi post-policitemia vera e mielofibrosi post-trombocitemia essenziale.
Ruxolitinib ha dimostrato di essere in grado di ridurre le dimensioni della milza e di controllare i sintomi della mielofibrosi in maniera più efficace rispetto ai farmaci tradizionali e al placebo (sostanza senza proprietà medicinali) con cui è stato messo a confronto.
Nei due studi clinici COMFORT I e COMFORT II, condotti in pazienti di diversi Paesi tra cui l’Italia, ruxolitinib ha determinato una riduzione dell’ingrossamento della milza in una buona parte dei pazienti, e questo beneficio si è mantenuto in circa la metà dei casi dopo tre anni di trattamento. In alcuni pazienti, dopo oltre 3 anni di trattamento, la fibrosi del midollo è risultata stabilizzata o ridotta rispetto alle condizioni di partenza.
L’efficacia del trattamento è risultata rapida: nello spazio di un mese si sono osservati notevoli miglioramenti di vari disturbi della mielofibrosi, come il prurito, la stanchezza, il calo di peso e la febbre.
Inoltre ruxolitinib è il primo farmaco per il quale è stato dimostrato un aumento della sopravvivenza dei malati di mielofibrosi.
Dall’analisi dei dati dello studio COMFORT II dopo 3 anni di trattamento, per i pazienti trattati con ruxolitinib è stata osservata una riduzione del rischio di morte del 52% rispetto alla migliore terapia convenzionale disponibile.
Per quanto concerne gli effetti collaterali, quelli più frequenti sono l’anemia e la riduzione del numero di piastrine (trombocitopenia). Si tratta di effetti coerenti con il meccanismo d’azione di ruxolitinib e sono correlati alla dose, per cui si possono gestire diminuendo le dosi del farmaco. Infatti ruxolitinib, come tutti gli altri JAK2 inibitori in fase di sviluppo clinico, non è specifico per la proteina JAK2 mutata ma può colpire anche la proteina normale, contribuendo quindi allo sviluppo della trombocitopenia e anemia.
Altri farmaci di questo tipo sono ancora in sperimentazione e saranno disponibili nei prossimi anni.
TERAPIE DEL FUTURO
Oltre a ruxolitinib sono in fase di sperimentazione anche altri inibitori di JAK e di altre proteine alterate fra cui mTOR.
Altri farmaci che in futuro potrebbero avere un ruolo nella terapia della mielofibrosi sono composti che agiscono direttamente sul DNA contenuto nelle cellule (chiamati inibitori dell’istone deacetilasi), come givinostat e panobinostat.
Qualità di vita
IMPATTO DELLA MALATTIA
Anche se il tipo e la gravità dei sintomi variano da individuo a individuo, la mielofibrosi è comunque una malattia cronica che peggiora gradualmente con il passare degli anni, compromettendo progressivamente le condizioni generali di salute.
Tuttavia un adeguato trattamento farmacologico, l’uso di alcuni semplici accorgimenti e il rispetto di poche regole di tipo generale, consentono di migliorare considerevolmente la qualità di vita dei malati.
Spesso è possibile ritornare a svolgere le attività di tutti i giorni (camminare, salire le scale, rifare il letto, cucinare, leggere, guardare la televisione) senza particolari problemi.
CONSIGLI PRATICI
Come regola generale è sempre utile adottare uno stile di vita salutare, seguire un’alimentazione corretta e se possibile svolgere una regolare attività fisica. Ma in pratica, cosa può fare un paziente con mielofibrosi per migliorare la propria qualità di vita?
Di seguito una serie di consigli utili.
Smettere di fumare è utile perché si sa che il fumo può fare aumentare il rischio di trombosi. Quindi non ha senso sottoporsi a delle cure per prevenire la trombosi e nello stesso tempo mantenere un’abitudine che contrasta gli effetti delle cure che si stanno facendo.
 Riguardo al cibo, chi è effetto da mielofibrosi tende a mangiare poco, perché l’ingrossamento della milza provoca mancanza di appetito e sensazione di sazietà precoce. Questi fenomeni si possono contrastare mangiando poco ma spesso e scegliendo i cibi preferiti e più appetibili. Una maniera di pensare alla propria salute decisamente piacevole!
Riguardo al cibo, chi è effetto da mielofibrosi tende a mangiare poco, perché l’ingrossamento della milza provoca mancanza di appetito e sensazione di sazietà precoce. Questi fenomeni si possono contrastare mangiando poco ma spesso e scegliendo i cibi preferiti e più appetibili. Una maniera di pensare alla propria salute decisamente piacevole!
L’attività fisica in genere fa sempre bene, purché ovviamente si tenga conto della propria età e delle condizioni fisiche generali, quindi senza esagerare. Una semplice passeggiata, soprattutto se fatta in un bel posto, è utile non solo al corpo, ma può migliorare anche l’umore.
Se si vuole fare sport a un livello un po’ più intenso non ci sono controindicazioni generali. Si devono però evitare gli sport che prevedono un contatto fisico, come il pugilato e il rugby, per l’alto rischio di emorragia legato alla mielofibrosi, e praticare con cautela gli sport in cui si rischiano cadute e traumi importanti, come lo sci e il ciclismo. In questi casi è sempre meglio usare il casco e gli altri dispositivi di protezione.
Il consiglio di lavarsi con acqua fredda e asciugarsi tamponando la pelle serve ad evitare il prurito, che è uno dei disturbi più fastidiosi della malattia. Il prurito può verificarsi in ogni parte del corpo e diventa più intenso al contatto con l’acqua, soprattutto se è troppo calda. Per questo è sempre meglio lavarsi preferibilmente con acqua fredda o tiepida. Il fatto di asciugarsi tamponando la pelle, anzichè sfregare, serve ovviamente e ridurre lo stimolo diretto sulla pelle che può scatenare il prurito.
Anche gli ultimi due consigli, mantenere la pelle bene idratata ed evitare di indossare dei vestiti troppo aderenti o di materiale sintetico, servono ad evitare l’aggravamento del prurito. Sono degli accorgimenti pratici estremamente semplici e allo stesso tempo molto efficaci.
Oltre a questi consigli pratici per migliorare la qualità di vita del malato, è sempre necessario effettuare controlli periodici per monitorare sia lo stato di salute generale sia l’efficacia delle terapie farmacologiche, in modo da poter intervenire al primo segnale di peggioramento.
